扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
 今日,百时美施贵宝(BMS)和bluebird bio公司联合宣布,已向美国食品药品监督管理局(FDA)提交双方联合开发的CAR-T疗法idecabtagene vicleucel(ide-cel,又名bb2121)的生物制品许可申请(BLA)。这是一款靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR)T细胞免疫疗法,用于治疗复发/难治性多发性骨髓瘤(R/R MM)成人患者。本次提交提供了化学、生产和控制(CMC)模块的更多详细信息,以解决2020年3月初始BLA提交后FDA在2020年5月提出的未满足的监管要求。
今日,百时美施贵宝(BMS)和bluebird bio公司联合宣布,已向美国食品药品监督管理局(FDA)提交双方联合开发的CAR-T疗法idecabtagene vicleucel(ide-cel,又名bb2121)的生物制品许可申请(BLA)。这是一款靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR)T细胞免疫疗法,用于治疗复发/难治性多发性骨髓瘤(R/R MM)成人患者。本次提交提供了化学、生产和控制(CMC)模块的更多详细信息,以解决2020年3月初始BLA提交后FDA在2020年5月提出的未满足的监管要求。
MM是一种恶性的浆细胞疾病,其特征为骨髓浆细胞异常增生,并伴有单克隆免疫球蛋白过度生成。异常浆细胞在骨髓中聚集,可在体内多处骨组织形成肿瘤。这些细胞不仅无法行使正常功能,产生的抗体还会导致骨髓无法生成健康的血细胞。除此之外,患者还会伴有多发性溶骨性损害、高钙血症、贫血、肾脏损害。尽管目前多发性骨髓瘤具有多种疗法,但仍然会有很多患者对所有获批疗法产生抗性,发展创新疗法治疗多发性骨髓瘤十分重要。
B细胞成熟抗原(BCMA)是一种在多发性骨髓瘤的癌细胞上普遍表达的蛋白质,它是这种侵袭性血液癌症的重要潜在靶点。ide-cel可以识别并与多发性骨髓瘤细胞表面的BCMA结合,进而导致CAR-T细胞增殖和分化,并随后对表达BCMA的细胞进行杀伤。此前,ide-cel已获得FDA授予的突破性疗法资格,并获得欧洲药品管理局的PRIME认定。
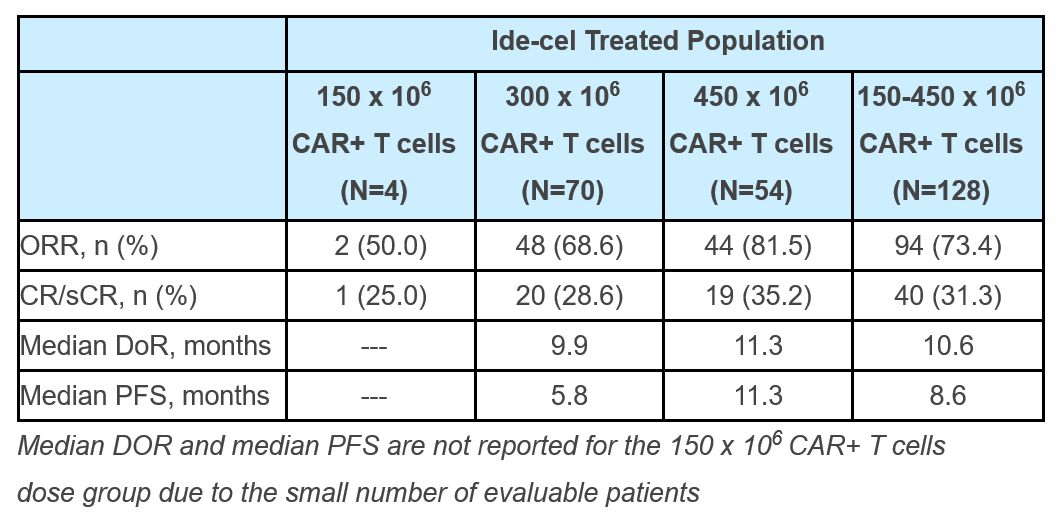
▲Ide-cel的主要疗效数据(图片来源:参考资料[2])
该项上市申请的递交是基于名为KarMMa的关键性单臂、开放标签2期临床试验的积极结果,参与该试验的R/R MM患者都已经至少接受过免疫调节药物(IMiD)、蛋白酶体抑制剂(PI)、和抗CD38抗体的治疗,并且对疗法产生耐药性。其中94%的患者对抗CD38抗体疗法产生耐药性,84%的患者具有三重耐药性。试验结果表明,在总计128名能够评估疗效的患者中,患者的客观缓解率(ORR)达到73.4%,完全缓解率(CR)达到31.3%。在中位随访时间为11.3个月时,这些患者的无进展生存期(PFS)达到8.6个月。
两家公司表示,将致力与FDA合作,快速推动ide-cel的监管审评过程。我们期待这次申请能够一切顺利,早日为MM患者带来创新治疗选择。
参考资料:
[1] Bristol Myers Squibb and bluebird bio Announce Submission of Biologics License Application (BLA) to FDA for Idecabtagene Vicleucel (Ide-cel, bb2121) for Adults with Relapsed and Refractory Multiple Myeloma. Retrieved July 29, 2020, from https://www.businesswire.com/news/home/20200729005776/en
[2] Bristol-Myers Squibb and bluebird bio Announce Positive Top-line Results from the Pivotal Phase 2 KarMMa Study of Ide-cel in Relapsed and Refractory Multiple Myeloma. Retrieved March 31, 2020, from https://www.businesswire.com/news/home/20191206005463/en/Bristol-Myers-Squibb-bluebird-bio-Announce-Positive-Top-line
文章来源:药明康德
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。