扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们

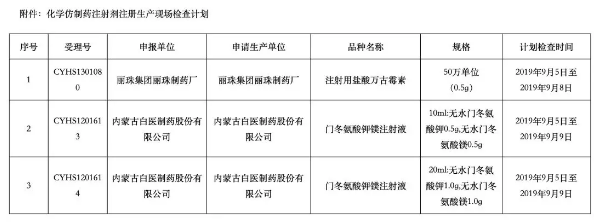
根据《药品注册管理办法》和《国家药品监督管理局关于加强化学仿制药注射剂注册申请现场检查工作的公告》(2018年第 20号)要求,我中心计划对注射用盐酸万古霉素等3个品种(规格)开展注册生产现场检查(详见附件)。如在通告的检查时间内注册申请人不能接受现场检查,需在通告后10个工作日内主动向我中心提出撤回现场检查的书面申请(邮寄或现场递交)。10个工作日后,注册申请人不得撤回现场检查申请。

联系电话:杜 婧 010-68441662,颜若曦 010-68441687
传 真:010-68441300
联系地址:北京市西城区文兴街1号院3号楼北矿金融大厦6层
邮 编:100044
特此通告。
国家药品监督管理局食品药品审核查验中心
2019年9月2日
文章来源:蒲公英
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。