扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
1、问:GMP106条规定:所有到货物料应该检查并与订单保持一致,并确认供应商已经质量管理部门批准。请问在药厂中这是什么样的流程?是怎样确定供应商经质量管理部门批准的?
答:①物料接收流程如下:
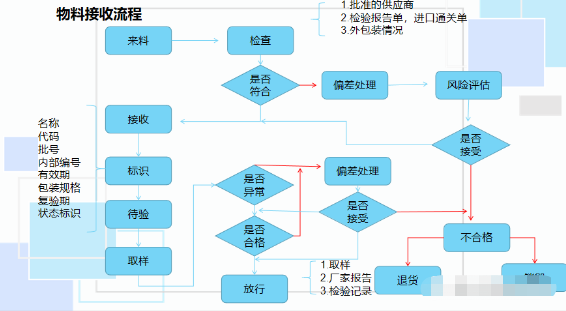
②供应商新增流程,新增后自然会加入合格供应商目录:
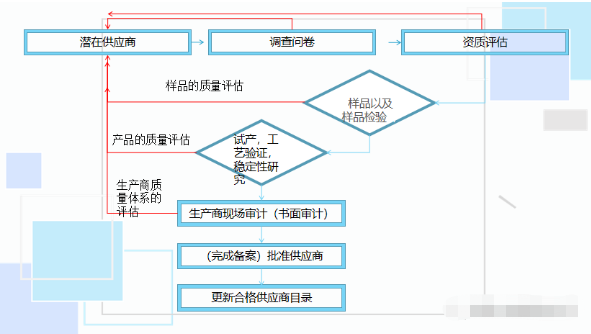
③质量管理部门应当向物料管理部门分发经批准的合格供应商名单,该名单内容至少包括物料名称、规格、质量标准、生产商名称和地址、经销商(如有)名称等,并及时更新。
2、问:2019年底制定了2020年度的供应商现场审计计划,一家都未审计,本想春节后加紧进行,却遇到疫情,不知道持续到什么时候。不知同行对这项工作有什么安排,今年怎么计划?到底还进行现场审计不?答:推迟吧,建议变更审计计划:①延迟对风险较低的供应商和承包商的审计,根据该物料产品质量及历史审计情况,合理地推迟到今年晚些时候或更长时间;②可改用调查问卷的方式进行审计(可额外增加问题,比如,公司是否配备充分人员进行生产、检验、包装或分销,或者是否发生人员减少?如果是,生产或检验的量是否相应的减少?该工厂实施了哪些其他控制措施来确保产品质量不受到负面影响?),如果该物料产品质量及历史审计情况令人满意,则此方法可能足以作为临时控制,直到可以安排现场审计;③通过视频会议与对方对接,了解对方质量管理体系运行情况。
4、问:供应商审计是否只能由质量部门人员执行?答:质量审计是质量部门人员的专有权力。在特殊情形下,其它部门(例如,采购、技术运营、R&D)亦可参与供应商审计,以支持供应商选择。这些访问如果没有质量部门人员参与,则不能代替审计。另外,对供应商进行最终批准是质量部门的职责。
5、问:原料药通过经营公司进行购买,原料药生产厂家不变的情况下经营公司发生变更,企业有必要做一个相关的变更吗?答:需要。同时从两个不同的经销商采购的同一个厂家的原辅料,也都要分别做供应商审计,并且相应的原辅料也应该使用不同的物料代码。这是因为不同的供应商,其储存和运输条件很可能存在差异,这个差异可能影响原辅料的质量,进而影响最终产品的质量。
7、问:公司研发物料和生产物料的供应商管理需要分开吗?答:分开管理较好,因为研发用物料,特别是小试阶段,变数较多,如果依据生产管理,那物料变更这块执行起来太累了。中试到大生产试验阶段,逐步靠近生产管理。
9、问:制剂产品原料供应商发生改变是否需要向药监部门备案?还是可以直接新增供应商?答:先公司内部走变更流程,然后做验证,稳定性考察等完成后,向省局申报补充申请,批准后方可使用新的供应商。
文章来源:蒲公英制药论坛
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。