扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们

延伸阅读:近十年FDA483警告信,趋势分析
备注:数据日期截至2019年11月30日。
又到了一年一度的总结时刻,和往年一样医药行业的2019年又是跌宕起伏,精彩纷呈的一年。
今年恰逢建国70周年,全国人民爱国热情空前高涨,《我爱你中国》这首歌在街头巷尾被所有人传唱,《我和我的祖国》成了国庆档电影票房之王,然而10月1日正当全国人民载歌载舞欢庆建国70周年之时,由上海医工院的一封警告信一石激起千层浪,在民族情绪高昂的背景下也激起了全国人民对美帝的愤怒。
可事实真的如大家所想的那样吗?
2018年的另一起大事件—缬沙坦事件在2019年持续发酵,华海不出意外也收到了FDA的警告信,且自己总部的API设施在今年五月份的检查中又被FDA出示了OAI,天宇的两个设施在四月份的FDA检查中也中枪,分别拿到了OAI,全球范围的召回进行得可谓相当惨烈。真不晓得华海和天宇何时能迈过这个坎!
欧洲方面华海的帽子好不容易摘掉了,但是齐鲁天和的帽子还没有摘掉。国内另一个制药行业的巨头海正位于椒江的两个设施又于今年7月收到了西班牙的不符合报告,在其内部架构交替变更之时还真是有点雪上加霜的味道!10月份法国给了江西东风无菌原料药不符合报告,11月份,华北制药华民又收到了克罗地亚官方检查无菌原料药的不符合报告,可以预见明年这几家大药企的出口会受到比较大的影响。
而药监官方方面,今年也是流年不利,欧洲药监局EMA因为英国脱欧的影响于1月份搬到了荷兰首都阿姆斯特丹,搬家的影响前前后后持续了有将近1年,一些非核心的任务被搁置或延期,而从12月24日开始FDA因为美国政府的停摆,也被迫停摆35天,创下了停摆最长时间新纪录!
在这里,也想问一下制药行业的同行们,这一年是否是您历史上最为艰难的一年?
但是会不会是未来五年内最为轻松的一年?
在这里我们所作的统计和记录是为了将来能更好地进行回顾和总结。
一、欧盟C GMP检查数据汇总分析
(一)、2018~2019年度欧盟不符合报告分析
2019年对于欧盟来讲是个动荡的一年,截至到2019年11月底,欧盟官方在2019年度只进行了2482次现场检查,公布了15份GMP不符合报告,远远低于历史水平,笔者对于这些报告进行了简单的统计分析。
从历史数据来看,欧盟官方的检查数量从2016年度一直到2018年都是处于增加的趋势,但是在今年相对于去年却下降了50%之多,相应的欧盟之外第三国的现场检查数量也明显减少,都处于5年内最低水平,具体数据请见表1,究竟是今年欧盟对药企的监管放松了?还是药企的GMP水平提高了?
笔者认为这恐怕受英国脱欧的影响更大,脱欧直接导致EMA搬到阿姆斯特丹,办公地点改变的导致大约25%的人员变动,从而会严重影响了EMA至少半年的正常运作,大约这是导致欧盟官方不得不暂且放松对制药企业的监管的主要原因。
但是从表2中统计的几个主要欧洲国家的检查次数来看,虽然脱欧搞得大部分欧洲国家鸡飞狗跳,但是好像并没有影响到MHRA对制药行业的监管,可见MHRA作为欧盟的老大哥,其地位和能力是毋庸置疑的,而其他几个主力国家的检查数量却都有了明显的下降。时间是治愈一切的良药,笔者相信随着时间的迁移,新的雇员慢慢都会就位,相信欧盟官方的检查会逐渐正常起来,让我们拭目以待明年的统计数据。
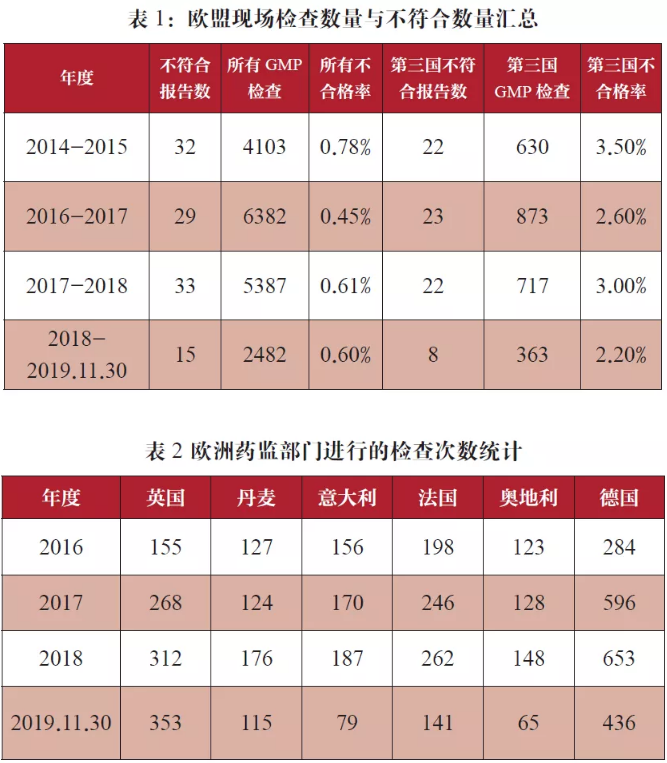
图1为欧盟现场检查全球不符合工厂国家分布,从图1可以看到,虽然同样受到英国脱欧的影响,不符合报告涉及工厂的所在国家也从11个减为7个,但是排名前五名的国家与2018和2017年度相比没有变化,仍然为印度、中国(西班牙并列)、英国,以及意大利(奥地利和丹麦并列),分别有4家,3家,2家和1家工厂。
结合图2看,在欧盟检查数量减少了一半的情况下,中国和印度无论是从不合格报告的数量还是比例上来看都仍然居于状元和榜眼的位置,中国作为一个制药大国,其一直处于上升的不合格率揭示了国内整体的GMP水平在世界范围内仍然还是有很大差距的,说明我们国家要想成为一个制药强国仍然有很长的路要走,而且从华海、齐鲁、海正、江西东风以及华北制药都有场地在近两年拿到了不合格报告来看,虽然也可能存在偶然因素,但是也能反映出GMP的要求是不断进步的,制药企业必须要一贯地、严格地持之以恒,才能尽量避免走弯路;
从目前的数据看印度的制药企业的整体情况变化不大,但是从FDA对印度企业的监管统计数据来看,今年FDA对印度企业并不友好,具体分析见第二部分,也许明年欧盟也会随之加大对印度药企的检查力度;而英国和西班牙一直以来都是欧洲监管水平和严格程度都比较高的国家,从进行检查的数量和结果来看,其整体GMP符合性水平还是非常高而且稳定的,意大利和奥地利同样也是处于一个比较稳定的状态。
而西班牙的不合格率看起来是有一个明显的增加,但是这个增长其实是因为检查数量的降低而造成的(只有去年的四分之一),所以实际上这并不能说明西班牙制药水平下降了,而且西班牙工厂的不合格报告都是西班牙官方自己检查的,反而更加说明西班牙的监管机构以及其制药企业GMP水平仍然是居于世界前列的。
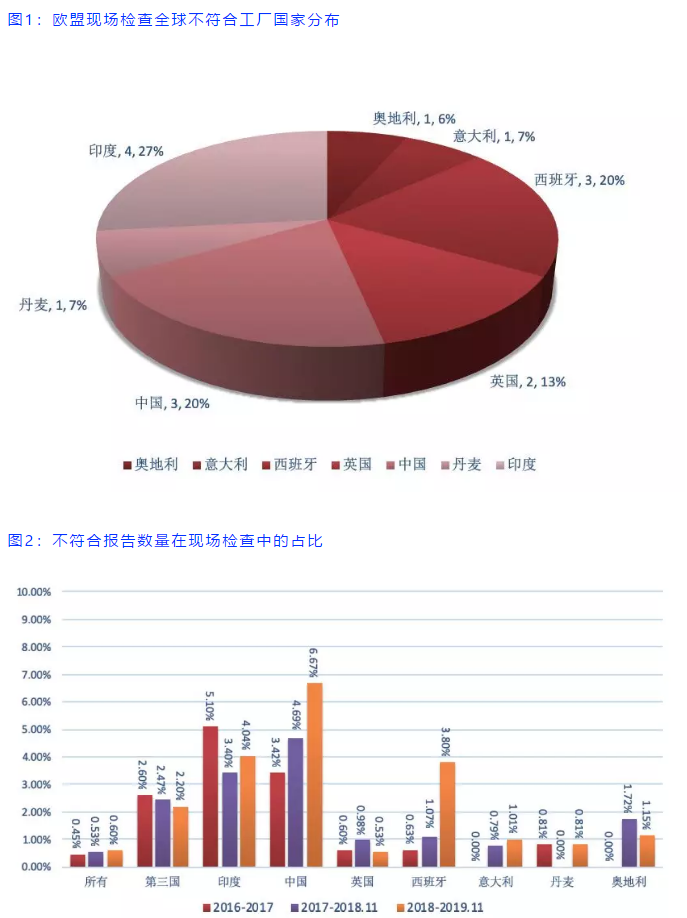
图3是在2019年发出不符合报告的官方机构分布,从图3可以看到,传统监管比较严格的欧盟成员国官方,发出的不符合报告还是最多的。
英国和法国一如既往处于前三的位置,而西班牙今年超越了去年的英国,取代了意大利,成为2019年度发布不合格报告最多(4份)的国家,而且也是西班牙历史上最多的一年,中国企业海正收到的不合格报告正是拜西班牙官方所赐。
所以鉴于其开具不合格报告数量的持续增多,强烈建议正在做或者打算做西班牙注册的中国药企要提高警惕,看下西班牙官方的不合格报告中提出的问题,在自己企业是否存在,但是无论如何如果只是为了通过认证那只能应付得了眼前一时,却并不是长远之计,只有不断修炼内功,提高自己企业的GMP水平才是良策。
而我们去年提到的给印度企业发了两份不合格报告的马耳他药监局,到目前为止今年共进行了20次审计,主要集中马耳他本国内(12次)和印度(6次),到目前为止还没有发布过不合格报告,但是从海外检查占比来看,马耳他进行的国外检查占到了他检查总数的接近一半,目前的重点是在印度企业,可见其对药企的监管也是比较严格的了。
而德国官方包括各州的药监机构还是一如既往的宽厚仁慈,在这么大的检查基数上,今年一封不合格报告都没有开出来,如果你的企业是在做德国注册,那你运气好了。
图3:2019发出不符合报告的官方机构分布
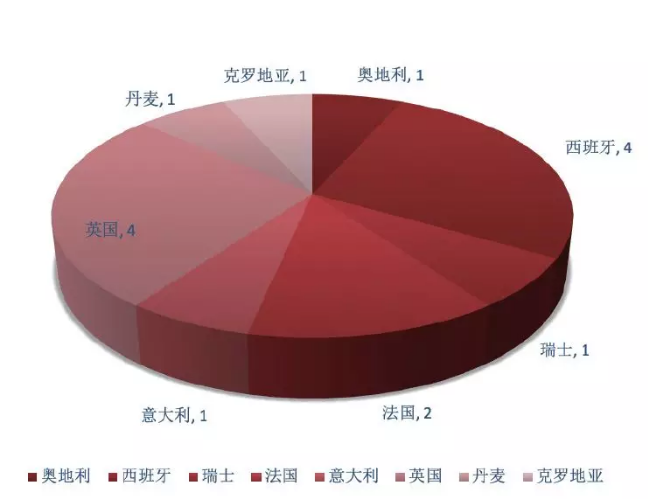
从图4可以看出,2018-2019年度的15份不符合报告中只有6份是发给制剂企业的,剩下的9份发给了原料药生产企业。
结合之前的数据,我们可以看到API企业是呈现增加的趋势,而制剂却呈现减少的趋势,而且今年API的不合格数量首次超过了制剂厂,也许这预示着从今年开始,EMA要加强对API厂的监管了,毕竟要想确保制剂的质量,API是源头。
然后我们再关注一下这9家在2019年度收到不符合报告的API工厂,包括了3家中国工厂(NCPC华民和海正,江西东风,其中两家为无菌API工厂)和2家印度工厂,剩余的4家都是欧洲工厂(西班牙2家,英国2家),由此也可以佐证,欧盟官方在整体上是加严了对API工厂,尤其是无菌API的监管。
而收到不合格报告的6家制剂工厂中有两家印度工厂,都是由英国药监局开具的,其他4家分布在奥地利,意大利,西班牙和丹麦,均由其自己国家开具,也许这提示欧盟官方的监管力度目前更多的放到了自己辖区内了,也可能是欧美官方互认后和美国官方交流提升的结果
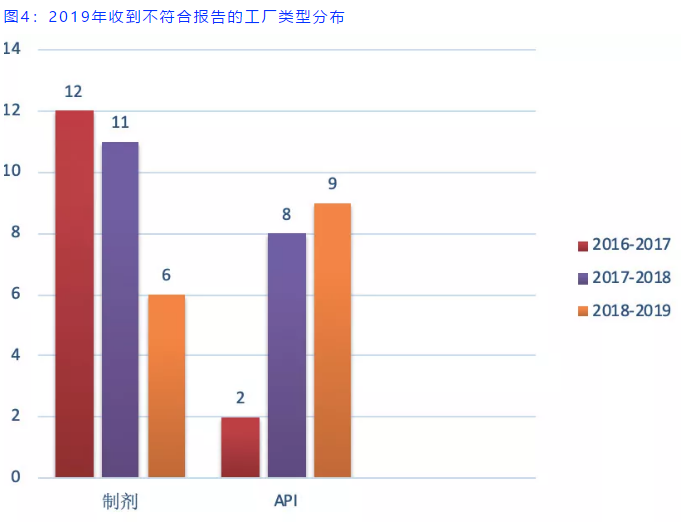
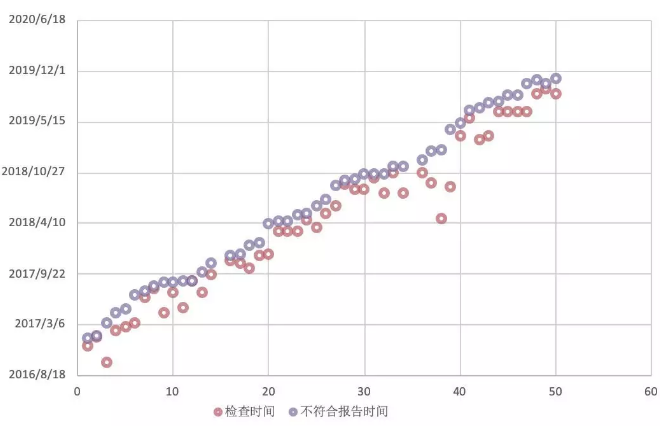
图5是欧盟官方检查日期和不符合报告发布的时间分布图,可以看出,在2018年上半年之前,检查之后公布不符合报告的时间间隔已经有越来越短的趋势。
但是从下半年开始直到2019年上半年,出现了明显的延迟,这段时间也正是EMA启动搬迁的阶段,经过了差不多1年的动荡期,受此影响,奥地利官方的检查从检查结束到发布报告竟然用了8个多月,而今年下半年往后已经逐渐回归正常的间隔,其中丹麦发出的不合格报告从检查结束到发布已经仅仅用了3周时间,估计2020年EMA的检查会逐渐密集起来,来弥补这一年的耽搁。
图5:欧盟官方检查日期和不符合报告日期分布图
由于欧盟发布的不符合报告并没有像FDA警告信一样明确列出缺陷条数及内容,有的报告中只有条数,而没有具体每条内容,或者只列出缺陷的主题,而没有具体条数,所以本文的缺陷分类中的“条”数并不代表实际具体缺陷“个”数,仅仅是根据报告列出的中的关键和主要缺陷个数或者主题个数进行粗略分析得到,所以用“条”字和 “个”以示区分,如有不妥之处,还望大家海涵。
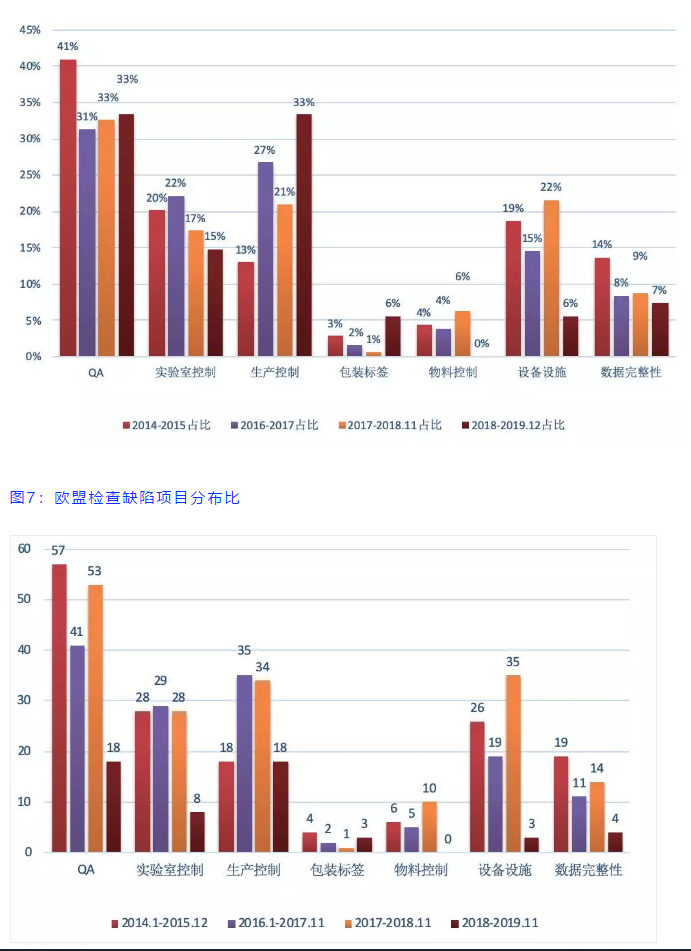
2018-2019年度的15封不符合报告中关键缺陷和主要缺陷以及数据完整性缺陷共计113条,我们只对其中列出了具体缺陷内容的54条缺陷进行汇总和分析,从图6和图7可以看出,和往年一样QA系统还是缺陷项最多部分,而生产系统和包装标签方面的缺陷有明显增加,QC系统、物料系统以及数据完整性的缺陷和往年持平。整体来看,生产和QA系统的缺陷数量相当。
生产控制方面,也许是沙坦事件的延伸,在设备清洗导致交叉污染风险方面的缺陷明显增多,所有交叉污染方面的缺陷都作为关键缺陷项列出,这与FDA的关注点不谋而合,而且华海和天宇都因为交叉污染的风险而被欧盟紧急检查,但是从这一事件我们可以看出欧盟官方对这类突发事件的处理态度和方法是简单而粗暴的,而且一直到现在,这件事情还发酵到欧盟要求所有生产企业对出口欧盟的产品进行评估并提交评估报告的要求,甚至还贴心的发布了评估报告的模板。
另一个例子是从2018年开始在中国爆发的非洲猪瘟病毒,老百姓们关注的是今年猪肉价格的一路飞涨,而欧盟今官方却已经关注到了肝素钠以及所有使用猪提取物制品来源的API(胆红素等)进行猪瘟病毒监测的要求,在猪肉涨价,猪瘟横行的今天的中国制药行业是否会发生类似2008年肝素钠药害事件,还有待我们高度关注和重视。
而无菌生产方面,设备及部件的灭菌,灭菌过程的温度和蒸汽的监控和检测,灭菌工艺的验证,模拟灌装,环境监测以及生产操作本身这些高风险的点仍然是欧盟官方检查的重点,在此提醒国内正在做或者打算做无菌产品欧美注册的厂家,如果上面提到的这些点你不真正熟悉欧美的相关指南的要求,就证明你并不是真正了解无菌生产工艺,建议还是不要被人忽悠了冒然就出手。
QA体系方面数据完整性问题,偏差和OOS的调查不彻底和无效CAPA的问题也占了很大的比重,这2个方面欧盟官方和FDA一样,也是非常关注的。
建议大家保持对于QC数据完整性重视的情况下,也不能放松对于偏差和OOS的管理,尤其要提醒下稳定性研究方面的OOS数据的调查,也是会列为主要缺陷的,在调查方面要特别需要注意调查的科学性和合理性,以及CAPA的有效性。
而在QC方面,方法验证不充分,记录的追溯性,OOS结果的报告,记录的受控等等老生常谈的内容仍然是检查的重点,也还是会被作为主要缺陷提出来。
图6:欧盟检查缺陷项目分布图
(二)、2015.1-2019.11欧盟检查中国企业汇总分析(仅分析EudraGMDP公开的检查数据)
基于自然年的已经公开的数据,我们汇总了过去五年的数据,当然2019年目前可以获得的数据截止日期是2019年11月24日(少一个月的数据)。从图8可以看出2019年的现场检查次数和2018年比也是明显减少了接近50%,即便考虑时间因素,2019年的现场检查次数也很难回到2015-2016年的检查次数水平,这个也暗示着2019年是欧盟监管明显宽松的一年。英国脱欧如果在2020年继续不能明朗的话,那么可以预期2020年欧盟的检查也将是维持在2019年的水平,检查次数相对来说处于宽松的水平。
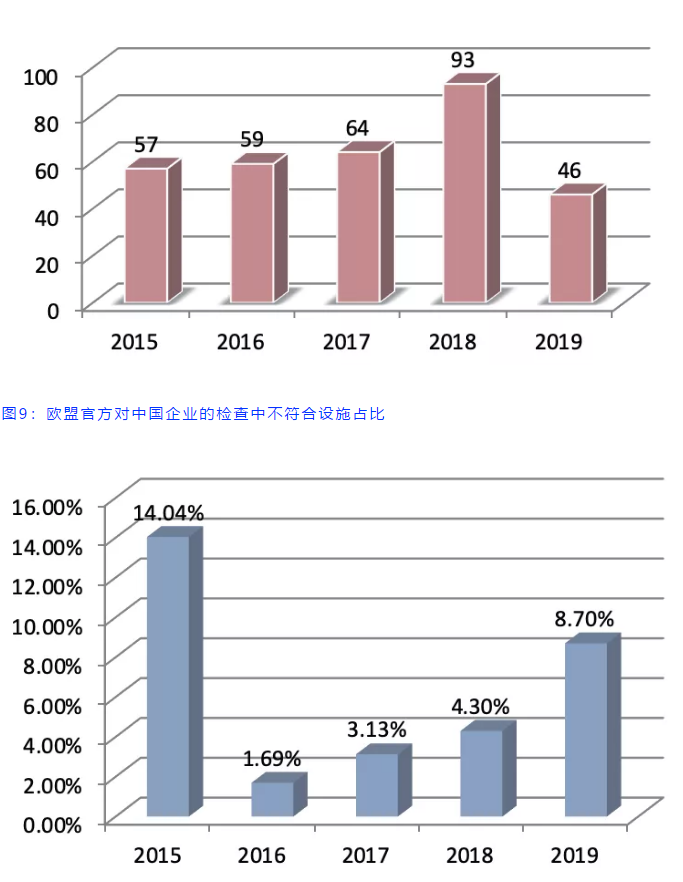
但是我们也从图9中看到,就不合格设施占当年的欧盟官方检查次数来说,实际2015年是欧盟现场检查在中国最为严格的一年,而从2016年到2019年,检查严格的趋势是逐步提升的。
也就是说虽然整体的检查次数在2019年比2018年下降了一半,但是实际检查到的企业拿到不符合信的绝对数保持不变,所以实际的不符合占比翻了一倍。
这个对那些不幸被检查的企业来说绝对是噩耗,而这个结果大概率是因为欧盟官方和美国官方一样开始采用风险评估工具对一些他们认为高风险的企业加大检查频率的结果。
虽然他们的检查频次少了,但是凡是出来检查的企业都不幸被他们的评估工具正确的预期了风险,的确存在较高的风险。
我们可以预期2020年一样这个不符合占比趋势会稳步的上升,是否会突破前期2015年风险评估工具应用前的最高记录,那就有待观察了。
图8:欧盟官方对中国企业的检查次数
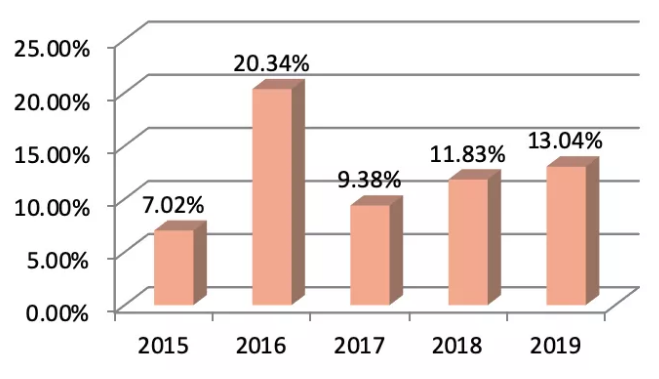
另外,很有意思的是,我们也从图10中看到,外资大公司在华的设施被欧盟官方检查的比例从2016年达到最高值,占比超过了20%,而后占比大幅度下降了50%原因是国内企业从2017年开始大量企业欧盟注册占比增加。
但是从2017年到2019年,外资在华设施被检查的占比也是稳步上升的。
大家都知道欧盟目前对设施检查的规则是持续大量出口,或是高风险的设施会被重点检查,外资在华设施被抽到检查的比例持续上升,也就更多的意味着,在华外企的现有这些设施更多的承担了出口欧盟的业务,且应该出口的产品都是高附加值高风险的产品类型,所以才会持续被欧盟官方检查。
当然,就这些设施中,唯一拿到不符合信的还是2015年GSK天津设施(天津史克),从2016年至今没有其他新的外资设施被欧盟官方检查给与不符合信。这个现象也暗示着,国内的外资合资企业,尤其是那些小分子生产设施,更多的参与到跨国大企业的全球生产布局中去了,这个对行业来说一个很好的趋势。我们一样预期在未来2020年,这个占比还会继续上升。
图10:欧盟官方对中国企业的检查中外资企业设施占比
文章来源:蒲公英
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。