扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们

介绍
原料药工厂中的多产品设备清洁要求进行清洁验证。清洁工作量会比较大。为了减少验证的工作量,可以采用最差情形方法进行验证。
采用分组法时,物质按类进行分组。
然后在每组中采用最差情形分级法选择各组中最差的情况。
对最差情形进行验证。至关重要的是,选择最差情形的科学合理性要进行记录。
本章介绍了所需要进行的工作、可接受标准和数据评估方法。需要强调的是,这只是一个指导性的例子,而实际情况下,设备、生产的物质和清洁程序可能有所不同,则可能需要采用与例中不同的解决方案。
最差情形分级优先性是用来支持清洁方法对组内所有原料药和化学物均有效的结论的,包括那些并没有进行单独检测的物质。
2 分组法
分组法的目的是让公司可以证明清洁验证方案中,对原料药进行最差情形分级具有科学合理性。首先要做的是进行分组和分小组----我们称为“分组法(括号法)”,在一个组中,再根据分级结果选择一个最差情形。分组流程应包括在公司方针中,或在SOP或相当清洁验证文件中。以下的例子中我们假定有一个多功能工厂、一个BP公司。
a) 设备链:
BP公司是一个多功能场所,从事化合物合成和分离(参见图1)。其设备被分为6条生产设备链,相互独立,用于不同用途(较早的原料药步骤、最终原料药精制、干燥等)。在A链中,可以生产9种物质,在B链中,可以生产9种物质,在C链中可以生产8种物质,在D链中,可以生产8种物质,在E链中可以生产10种物质,在F链中可以生产11种物质。如果不采用分组法和最差情形法的话,则需要对55种物质分别进行清洁验证。
进行分组的第一个标准是组内的物质是在同一条设备链中生产,并采用同一个清洁程序/SOP进行清洁。理想状态是每条链可以作为一个组来进行清洁验证。这样,理想状态下需要识别出6种最差情形。现实中,最差情形的识别可能会是两个极端情况(多于6个,但少于55个)。
BP公司
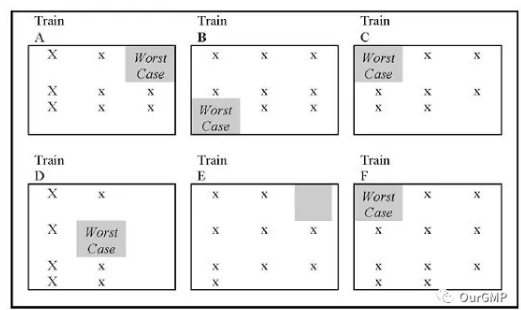
图1:清洁公司的理想案例(设备链1被作为第一组)给出了6个最差情形。
在此例中,组内主要级别是基于不同生产链的。以下设备分级不变:
TrainA
TrainB
TrainC
TrainD
TrainE
TrainF
b) 物质
如果公司有2个或更多设备链用于同一个生产目的(例如,更早的原料药生产步骤、最终原料药精制、干燥等),已选好了在每个设备链中生产哪个产品。在一个设备链生产哪些物质(起始物料、中间体或原料药)可以采用以下策略或组合策略来做选择:
l 在同一设备链里生产可以采用相同的清洁程序的物质
l 在同一设备链中生产治疗剂量很低和/或批量很小(以及相反情况)的物质
l 在同一设备链中生产ADE值非常低(以及相反情况)的物质
也可以选用具有最大灵活性的方式,但这样可能会使得残留限度非常低(比如如果需要清洁的物质有一个非常低的治疗剂量,后续物质有一个非常小的批量和/或非常高的日剂量),导致清洁时间会很长。在3中讨论了选用几个不同的清洁程序相比于选用同一个清洁程序的优缺点。在4中对不同策略的效果给出了进一步解释。
3 清洁程序
对于一条设备链,如果在其中生产几种物质,通常会有几种清洁程序。为了将所涉及的产品进行分组,第二个标准就是对同一组里的产品使用相同的清洁程序(方法)。
例如在以下情况下,可以认为清洁程序是相同的:
相同或等同发布的清洁批记录/清洁SOP
2. 相同溶剂、溶解度或相似特性
下表列出了采用几个清洁程序与采用同一个清洁程序的优缺点。
所有物质(选取最难清洁的物质做验证)采用同一清洁程序
|
+ 减少清洁验证的次数(可能只需验证一次) |
- 对所有物质都不是最优的清洁方法→平均清洁次数会比较多,同时溶剂消耗量大 - 一般对所有物质采用同一个较低的残留限度 |
优化每个物质的清洁程序
|
+ 降低平均清洁时间 |
- 增加清洁验证的最大次数 |
在案例中,BP公司评估了清洁程序,通过检查将其分为不同类别。同一类别中的物质采用相同方法清洁,采用相同的溶剂,通常其所含的化学物质相互类似(例如,盐、化学结构等)。在本例中,共包括四类清洁程序:
一类:水溶性物质
二类:甲醇可溶性物质
三类:丙酮可溶性物质
四类:根据溶解度制订的特殊物质特定级别
4. 调查和最差情况分级(WCR)/风险评估
进行最差情形分类研究/风险评估时,根据公司选择的可采用标准,对清洁验证程序中已有原料药进行优先顺序排列。BP公司选择了以下标准,该标准与在该工厂中生产的产品分子相关(公司应对自己的情况进行单独评估)
a) 最难清洁:生产所得的经验
b) 在所用溶剂中的溶解度
c) 可接受最低日暴露量(如果不能获得ADE/PDE数据,可以使用(参见第4章)其它药学(剂量)数据、OEL或毒性数据(LD50)
d) 最低治疗剂量(或毒性数据LD50)
为了形成书面证据来支持各标准分级的科学性,应进行研究(正式的风险评估)并形成书面的正式报告。每个标准中,要列出分级组所对应的描述性术语。如果可能,应从科学文献中选取相应的术语描述(例如溶解性和毒性)。其它情况下,分类也可以根据公司的科学研究和在清洁工艺方面积累的经验(即“生产经验”)。
BP公司选择根据一份正式的方案进行最差情形分级(WCR),对清洁情况进行分级并记录分级结果。在风险评估报告中,对结果,包括WCR,和结论进行综述。
a) 最难清洁---生产中得出的经验
分级可以使用的一个标准是生产中获得的关于该物质被清洁难度的经验。建议通过与操作人员和主管沟通进行该项研究。可以采用了一份标准化问卷,让操作人员和主管在问卷中标出答案,从问卷统计中找出最难清洁物质,然后根据以下三级进行分级。人们的观念可能会有主观性,因此,还需要有科学合理性来支持本方法。
分级
1==易清洁
2== 一般(中等难度)
3==难清洁
b) 溶解度
溶解度分级应根据物质在清洁用溶剂中的溶解度来分级。下表中给出了推荐的分级数及相关解释。描述性术语在USP24第53页“参考表格”(描述和溶解度,2254)中可以找到。
|
分组 |
所包括的描述性术语 |
一份溶质所需的溶剂份数,以重量计 |
|
1 |
极易溶解 易溶 |
小于1份 1-10份 |
|
2 |
可溶 略溶 |
10-30份 30-100份 |
|
3 |
微溶 极微溶解 几乎不溶 不溶 |
100-1000份 1000-10000份 大于10000份 |
c) ADE或PDE理念
可接受日暴露剂量界定的是在对健康不产生副作用的前提下,患者在终生时长内每天可以暴露于该物质的浓度限度。
下表中给出了一个分级数的例子及解释:
|
分组 |
ADE/PDE |
|
1 |
>500μg |
|
2 |
100-500μg |
|
3 |
10-99μg |
|
4 |
1-9μg |
|
5 |
<1μg |
如果不能获得ADE/PDE数据,也可以使用其它药学(剂量)、OEL或毒性数据(LD50)。
d) 治疗剂量
治疗剂量的研究一般是根据口服和/或注射数据的。如果无法获得治疗剂量,可以使用对应的毒性数据(根据公司程序进行再次计算)。下表给出了一个分级数的例子及其解释:
|
分组 |
包括给药间隔(最小治疗剂量) |
|
1 |
>1000mg |
|
2 |
100-1000mg |
|
3 |
10-99mg |
|
4 |
1-9mg |
|
5 |
<1mg |
5. 最差情况分级
所有物质按设备类别(设备链)和清洁类别(清洁程序)进行科学的矩阵列表。每个类别的组合被作为一个组。在进行分组时,可以开始最差情形分级(WCR)。在一个组中,至少要验证一个最差情形的清洁验证。以下为清洁公司的分级程序举例,实践中可以使用。
a) 分级程序
在最差情形分级过程中,对每个设备类别中每个物质的研究结果进行总结。如果清洁程序的评估结果显示有些物质需要独特的清洁程序,则这些物质作为一组(每个组员均是最差情形)。
如果在一个清洁类别(设备链/单个设备)中的所有物质均需要进行检测,则每个物质适用不同的限度。如果组中只有一些“最差情形”需要检测,则应按以下策略进行检测。如果采用了按优先顺序排列选择最差情形,则一般适用以下方法。
通用残留限度选择
评估最低计算限度用于所有用物质是否合理。如果合理,则该限度可以作为特定设备的通用限度。如果发现最低限度太低,不能作为所有物质的通用限度,则需要对第二低限度进行评估,以此类推。
清洁工艺验证标准
1. 对于具有通用限度的物质,针对每个清洁方法要检测具有最低溶解度的物质(在清洁溶剂/溶液中)。如果不止一个物质满足该标准,则应根据最难清洁经验选择一个物质用于通用标准检测。
2. 所有不能落在“括号”中的物质必须单独验证
b) 分级评估
可以根据签发的方案对最差情形进行分级。在方案中,要说明分级的方法和流程。可以使用7.4 a-d中所述的可用调查方法(可以附于方案或报告中,支持分级的合理性)。对于每个设备类别(例如干燥器),可以建立一个矩阵系列。作为案例,BP公司在下表中选择了设备链A,制订了一个正式的分级矩阵,为设备链A中生产的物质建立了两个清洁类别。所有类别在矩阵表中引入作为一列。
|
物质 |
清洁方法分级 |
a):*最难清洁 |
b): 溶解度 |
c): ADE |
d): 治疗剂量 |
|
E |
III |
2.3 |
1 |
4 |
3 |
|
F |
III |
2.2 |
1 |
2 |
4 |
|
C |
III |
2.1 |
1 |
3 |
2 |
|
L |
III |
1.9 |
1 |
3 |
3 |
|
O |
III |
2.8 |
2 |
2 |
3 |
|
M |
III |
2.5 |
2 |
2 |
3 |
|
P |
I |
2.2 |
1 |
2 |
3 |
|
R |
I |
2.6 |
2 |
3 |
3 |
|
T |
I |
1.8 |
1 |
2 |
3 |
*各数值是由操作工和主管回答不同问题的主要值。
在该设备链中生产的产品使用了两种清洁方法(I类和III类)。
因此,需要分为两组来进行验证。
III类中最差情形产品(用于验证研究)为O物质(溶解度2和最难清洁 2.8)
I类中最差情形产品(用于验证研究)为R物质(溶解度2和最难清洁2.6)
在两种情形下,均需要计算活性最高物质的限度(ADE4)。
如果无法获得ADE值,则根据活性最强的物质计算(治疗剂量4)。
如果采用ADE4或治疗剂量4可以计算所有产品的限度,则可将该限度用两组产品。
如果采用ADE4或治疗剂量4所计算出的限度太低,有的产品不能达到,则应考虑将E物质和F物质单列为一组,或在专用设备中生产。
剩下的组的限度应根据活性最强的物质(ADE 3 或治疗剂量3)来计算限度。
如果一种物质其优先级为最高,但不常生产,可以同时测试该物质和第二高优先级别的物质,以检查清洁是否对该类中其它所有物质均已足够。这样,最高优先级的物质会在第一次生产时进行测试。
WCR和风险评估一般会形成一份报告,其中包括对清洁验证程序所涉及的物质界定优先级别、进行分类情况。建议将完整的应用背景调查及其批准情况附入清洁验证方案或报告中。
c) 重新分级
对WCR也要实施变更控制。如果分级条件进行了变更,则要进行重新分级。以下列出了需要重新分级的例子:
l 变更清洁方法
l 变更工艺
l 变更/增加新产品
l 变更/增加新设备
在重新分级后,建议签发一份正式的控制文件,其中包括一份最差情况清单或表格,与原始分级所用的型式相同,在其中列出所涉及的物质/设备/方法结果。
文章来源:荀令君18 OurGMP
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。