扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
 1、内部质量控制
1、内部质量控制
是指实验室内部采取的以比对分析、跟踪以及对实验室工作的连续性控制计划。这是实验室质量保证的核心和基础,通过对检验人员、操作手册、检测环境、设备仪器及其功能检测、培养基试剂染色液等质量控制、检验过程的质量控制、标准菌株、以及实验室安全防护等方面的要求来进行的。这方面的内容包含微生物检测实验室日常运营的方方面面,一个健全完整的实验室应当在这些方面满足要求。
1、对于检测人员,应当具备相应的技术能力,并可以提供具备相应技术能力的证明,比如相应的证书等。CNAS-CL09中明确要求:实验室从事微生物检测的关键检测人员应至少具有微生物或相关专业专科及以上学历,或者具有10年以上微生物检测工作经历。这些都是对实验室检测人员的客观和硬性的要求,另外实验室检验人员还应具有高度的主观判断力,根据个人的技能、经验以及细菌学的专业水平可以对实验操作以及实验结果进行判断和分析。同时,实验室还应当有相应技术能力的人负责实验室内的技术工作,并设立质量监督员。
2、实验室的操作手册,是指实验室应当有一套系统的文件要求,包含实验室运营的各个方面,包括但不限于各级人员的职责和权限、实验室安全措施、样品采集和处理指南、培养基和试剂的配制方法等。实验室的操作手册是纲领性的文件,并且不是一成不变的,在实验室发生改变或者有重大变动时,也应当相应的修改操作手册以适应实验室的运营。
3、对于检测环境的要求,应当满足国家标准,要求检测室内足够宽敞、通风并有良好的照明,检测室内墙面地面采用易清洁的材料,可以根据工作内容将检测室加以分用,设立专用房间。
总之实验室的构造必须满足GB 4789.1-2016中要求。另外,各区域也应当各自的环境要求,并需要做好相关的记录,例如样品存放区、检测用无菌物品存放区应当监控温湿度并做好记录;无菌室应当按一定频率监控微生物指标并记录等,这些监控频率也都应在实验室操作手册中作出明确的要求。对于各功能间也应布局合理,其中准备区域、培养区域、检测无菌区域应尽量分开,各区域也应做好标识。
4、实验室的仪器设备,应当能够满足开展相关检测项目的要求,并制定相关设备仪器的作业指导书,关于一些特殊的设备仪器,例如蒸汽压力灭菌器等,需要人员取得相应的设备操作证书方可进行操作。
仪器设备的存放环境也应满足仪器本身使用要求,例如天平要放置在无振动无气流影响的水平台面;显微镜的放置环境要求无振动、避免灰尘、防潮等。
另外,仪器设备也应定期进行鉴定校准并记录其运行状况,维修后的仪器设备应当进行再校准,经检定后才可重新投入使用,并且整个维修和检定过程都应形成详细完整的报告。
下表是部分仪器设备检定和核查要求:
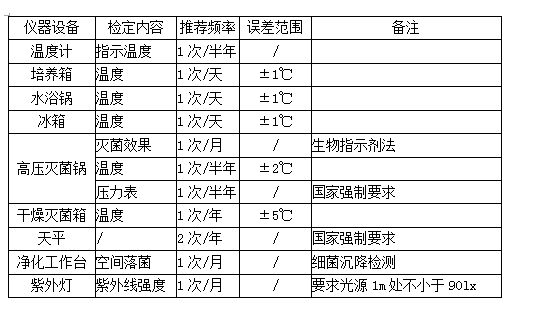
以上的校准、检定和核查,都需要详细的进行记录,并给出明确的检定结果鉴定。
5、常用培养基和试剂质量控制。首先要从培养基的物理、化学及生物学指标进行鉴定。例如培养基的感官,颜色级透明度;培养基的pH,以及无菌试验、生长率实验等。
商品化培养基存放环境也应满足培养基要求。培养基的配制过程必须统一标准,添加剂的剂量、pH以及灭菌时间或温度都须遵照规定,培养基名称、每批配制量、配方、配制日期和配制人员姓名都必须详细记录。另外配置培养基过程中使用到的仪器设备必须是经过检定的。
配制好的培养基保存环境应为0-4℃,如制成平板组需要用塑料袋包装好至于0-4℃环境保存,但若是含有高浓度胆盐的培养基应当存放在10-15℃的环境中,值得注意的是,配制好的培养基(尤其是糖发酵管)不宜久放,防止培养基会吸收空气中的二氧化碳导致培养基变酸影响细菌生长。
6、试剂的管理要求与培养基基本相同,下表是部分常用试剂进行阴性阳性检定时用的菌株。
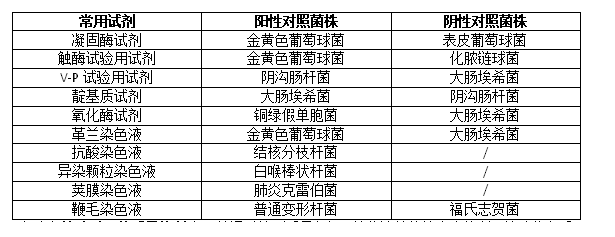
7、实验室检验过程的质量控制,也可以通过检测质量保证、菌落计数的精密度控制、菌种鉴定质控等几个方面来进行保证。
8、检测质量的保证是实验室最基础的能力,即保证样品检验过程的准确性,实验室应定期使用标准物质进行实验室内部的质量控制,也可参加实验室间的比对或能力验证。
另外,使用相同或者不同的试验方法对相同样品进行重复检验来验证实验室的检验过程也是常用的方法。对于计数的精密度也应做出明确的要求,以下是推荐的几种情况下计数的准确度判断:
同一平皿重复计数误差应小于7.7%;实验人员之间用同一平皿重复计数误差±18.2%;自身同一梯度平行加样两皿间相对误差小于7.7%,实验人员之间用同一梯度计数误差±18.2%,不同梯度这间菌落计数最终误差小于7.7%。这是推荐使用的重复计数的要求,实验室也可以根据实验室情况来确定实验室内部的误差允许范围,但误差范围也不应定的过大。关于计数精密度控制也建议每月进行1次。
9、实验室应当制定标准菌株的保存及使用规范,这个规范也可以包含于实验室操作手册中。其中标准菌株要求是形态、染色反应、生理生化及血清学特性典型而稳定的菌株,要求实验结果重复性好,不易发生变异的,通常来源于专门的机构,例如ATCC、CMCC、CICC等。
常用的菌种保藏方法包括冷冻干燥法(菌种保存中心常用)、冷冻保藏法、培养基保藏法等,各种保藏方法各有其优劣点,实验室可根据实验室内的条件选择相应的保存方法。近年来兴起的冷冻瓷珠保存法因为操作简单、并且保存时间长等优点,已经逐渐成为实验室主流的保藏菌种的方法。
10、最后,实验室的安全防护也不应忽视。首先实验室的管理人员以及实验人员必须了解相关工作有关的危险,对于新员工以及检测方法出现改变或启用新设备时尤其需要注意。检测过程中产生的废弃物要经过处理才可废弃,例如致病菌检测过程中使用的培养基、鉴定试剂等要经过灭菌后方可废弃。同时,进行致病性微生物相关工作的房间入口处必须要有生物危害的警示标志。
总之,实验室的生物安全管理应当符合GB 19489-2008里的要求。
以上内容基本涵盖了食品微生物检验实验室的 内部质量控制,除了这些,还应定期开展实验室间的质量评价。实验室内部质量控制是质量保证体系的重要组成部分,实验室应参加外部的质量控制活动,并且对于实验室内开展的每一项检测均应参加相应的实验室间质量控制。
2、实验室外部质量控制
具体包括外部机构对实验室进行的一系列的审核以及实验室的检测能力验证。前者的检查项目包括人员的资质以及相关培训,仪器设备的使用、保养和维修校准记录,培养基和试剂的配制记录、保存方法、灭菌质量,操作手册的执行、检测方法和操作规范性,实验室相关环境等等。
后者目前国内外广泛采用的方法是用模拟食品标本做质量评价,主要评价实验室在病原菌的分离、鉴定试验等方面的工作情况。由质控管理机构发放模拟标本或菌种,实验室按照日常的操作方法进行相应的分离鉴定试验。实验室完成鉴定后在规定时间内将检测结果反馈至参考实验室,质控管理部门会对质控结果进行统计分析,将实验室的结果与标准进行比较和统计分析,并作出评估,反馈评估报告,确定实验室相关的检验能力。实验室也要根据评估报告对实验室内部存在的相关问题进行整改,以符合相关的要求。
在微生物检验操作过程中,要保证检测环境(如超净台、检测室)以及所用工器具的洁净程度,同时保证人员各种操作的规范性,尽量保证其无菌性,防止因人为原因操作失误而出现误差结果,同时在适宜温度进行培养,为合理决策和指导生产提供依据。
为保证检测结果的准确性,我们应做好以下几个方面。
一、培养基的灭菌及使用
1、每次配制时,要注意其生产日期是否在保质期内,查看其开瓶日期及瓶口密封性,保证其未变质,并且未吸潮。
2、培养基配制时,称量要准确,包括盐水的分装要准确。
3、一定要保证现配制现灭菌,未灭菌的配好培养基不能长时间放置,更不可隔夜。
4、灭菌时要保证恒温、恒压,同时要保证有效的灭菌时间。
5、灭菌过的培养基要冰箱保存,可保存一周,一般不超过 3 天。而且要遵循“先入先出”原则,先配制的要先使用。
6、在使用时,要根据当班次的使用量,用水浴锅先将培养基溶化为液态,然后及时调低水浴温度(先化好的可从水浴取出,放在水浴锅锅盖上)待用,千万不可长时间使培养基处于高温状态。
7、做产品微生物检测时,倾倒培养基温度在 45℃左右,不可过烫,避免将菌烫死;也不可过凉,化好的培养基又结块凝固,不便于观察结果。
8、每瓶培养基均要做空白。
9、尽量集中做样,避免频繁打开同一瓶培养基瓶塞,增大培养基的污染几率,出现误差结果。
10、培养基剩余过少时,可先将其倾倒成空白用板。
二、检测环境的维持
大环境(检测室):
(1)检测时,窗户和空调要关闭,或用酒精对房间进行喷雾消毒,避免房间内空气流通影响超净台内部环境(最好在有通排风系统的恒温恒湿无菌间进行操作)。
(2)如果在原来的原料微生物检测室进行检测,要定期开启紫外灯,对房间进行杀菌。
小环境(超净工作台):
1、定期清洁初效过滤器,要及时更换。
2、检测前,将超净台内部进行清洁,用 75%酒精进行擦拭消毒,并提前半小时将超净台紫外灯打开,对超净台内部环境进行杀菌。
3、关紫外灯,开风机,调整合适进风量,风量不可过低。
4、每次检测后,要对超净台内部进行清理、清洁,并用 75%酒精进行擦拭消毒。
5、紫外灯根据其使用寿命要及时更换。
6、检测同时,要做上相应菌落检测的环境空白。
7、检测区域的选择:
a、一般在距离超净台外沿的 1/3-2/3 区域进行无菌操作;
b、要在酒精灯火焰的外焰保护区域进行操作。
三、工器具的洁净度
1、玻璃器皿:采用干热灭菌方式进行灭菌。
2、检测用剪刀、勺子等物品要做到检测专用,不可与其它操作器具混用,使用时,先用75%酒精消毒,再采用灼烧方式进行灭菌。
3、接种针(环)采用灼烧方式进行灭菌,但要注意检测时要先将接种针(环)进行冷却。
四、样品的采集及检测
1、保证采样器具的无菌性
(1)玻璃器皿:采用干热灭菌方式进行灭菌,保证恒温、时间足够(但不可时间过长,容易导致玻璃器皿易裂纹而报废)。
(2)取样筐:使用前要用75%酒精进行喷洒消毒。
(3)取样勺:要保证其清洁消毒,清洁后用75%酒精进行擦拭消毒。
(4)取样袋:可先用酒精进行擦拭消毒,再在超净台用紫外灯照射消毒,(包装车间要在传递窗用紫外灯照射消毒)。
(5)电子称表面用 75%酒精消毒。
2、人员操作
(1)保证手部的清洗、消毒:取样前及检测前都要先洗手再消毒。
(2)取样要具有代表性(随机样、目的样、综合样)且要标示清楚。
(3)取样完毕,不可在车间逗留,要及时将样品放入超净台,对其外表面进行紫外灯照射消毒。
(4)在要求的检测区域进行操作。
(5)检测前,要用 75%酒精棉球对样品袋口部进行擦拭消毒,再开口。
(6)往盐水瓶加样品时,要注意勺子或袋子尽量不接触瓶口。
(7)样品计量要准确,稀释倍数也要准确(1mL 吸管不允许将管口敲掉),进行 100 倍稀释时,1mL 吸管要伸入盐水中,不可以将样品从管壁流下去,同时要避免将管底部捅破。
(8)盐水温度以 40℃左右为宜,不能过热,会将部分微生物烫死;也不能温度太低,不能将样品溶解完全。
(9)进行稀释时,要摇匀,保证溶液的均一性。
(10)倾倒平皿时,要注意培养基瓶口不要接触到平皿;倾倒的培养基要适量,不可以太少,在培养过程中易干掉,微生物亦死亡,以 15mL 左右为宜。
(11)做大肠菌群样时,要提前将乳糖胆盐培养基培养管按需要量备好,放入超净台对外表面进行紫外线灭菌。
(12)接二步时,要注意先将接种针(环)进行冷却,避免出现接不上菌落的情况,导致无法判断、确认。
(13)检测完毕,及时放入相应培养箱进行培养,并清理清洁超净台。
五、微生物的培养
1、在培养过程中,要随时监控培养箱温度,保证其在适宜的温度进行培养。
2、要按照《微生物检验规范》要求及时观察结果,出现异常,要及时分析原因进行反馈。
文章来源:实验与分析
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。