扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
GMP附录-细胞治疗产品
(征求意见稿)
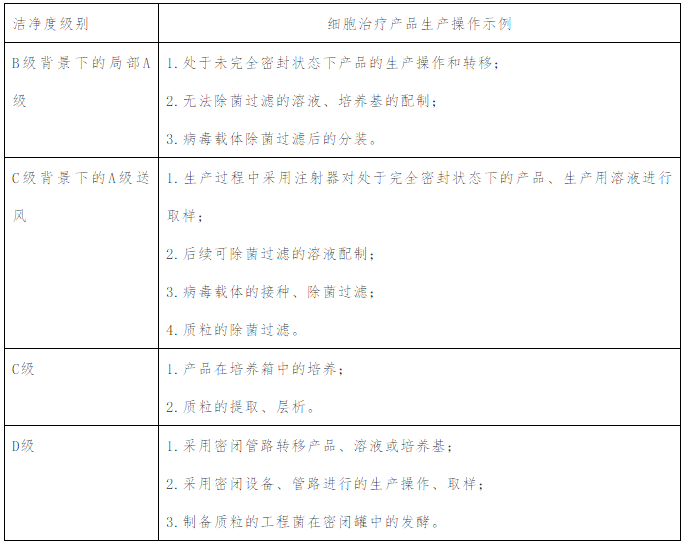
第七条 【生产人员】生产负责人应当具有相应的专业知识(如微生物学、细胞生物学、免疫学、生物化学等),至少具有三年从事生物制品或细胞治疗产品生产或质量管理的实践经验。第八条 【质量人员】质量负责人和质量受权人应当具有相应的专业知识(如微生物学、细胞生物学、免疫学、生物化学等),至少具有五年生物制品或细胞治疗产品生产、质量管理的实践经验,从事过生物制品或细胞治疗产品质量保证、质量控制等相关工作。第九条 【人员安全防护培训】从事细胞治疗产品生产、质量保证、质量控制及其他相关人员(包括清洁、维修人员)应当经过生物安全防护的培训,尤其是经过预防经供体材料传播疾病方面的知识培训,以防止传染性疾病的病原体在物料、产品和人员之间传播以及对环境潜在的影响。第十条 【人员活动限制】生产期间,未采用规定的去污染措施,从事质粒和病毒载体制备和细胞治疗产品生产的人员不得穿越不同的生产区域。 第四章 厂房、设施与设备第十一条 【厂房分区设计】细胞治疗产品、病毒载体和质粒的生产应当分别在各自独立的生产区域进行,并配备独立的空调净化系统。第十二条 【阳性供体材料生产厂房要求】含有传染性疾病病原体的供体材料,其生产操作应当在独立的专用生产区域进行,并采用独立的空调净化系统,保持相对负压。第十三条 【密闭系统】宜采用密闭设备、管路进行细胞治疗产品的生产操作;密闭设备、管路安置环境的洁净度级别可适当降低。第十四条 【隔离器】同一生产区域有多条相同的生产线,且采用隔离器的,每个隔离器应当单独直接排风。第十五条 【生产操作环境的洁净度级别】细胞治疗产品、病毒载体、质粒的生产操作环境的洁净度级别,可参照表格中的示例进行选择。
第十六条 【隔离贮存】含有传染性疾病病原体的供体材料和细胞治疗产品应有单独的隔离区域予以贮存,与其它仓储区分开,且采用独立的储存设备,相应的隔离区和储存设备都应当有明显标识。
第二十五条 【批的划分】单一供体、单次采集的供体材料在同一生产周期内生产的细胞治疗产品为一批。
第二十六条 【培养基模拟试验】病毒载体和细胞治疗产品无菌生产操作的培养基模拟试验应当符合以下要求:
使用相同设备和工艺步骤生产的不同产品,可采用括号法进行培养基模拟试验,模拟某些生产操作的极端条件;如采用矩阵法进行培养基模拟试验,应当模拟相似工艺步骤的最差条件;采用联用方法的,应当说明理由及合理性,模拟应当包括所有的无菌生产操作及最差其条件、所有生产用的设备类型。
第二十七条 【工艺验证】采用自体供体材料生产的细胞治疗产品,其工艺验证应当至少符合以下要求:
第二十八条 【病毒载体和质粒工艺验证】病毒载体和质粒的生产应当进行工艺验证,至少包含三个连续的完整工艺生产批次。
第二十九条 【生产中污染和交叉污染的防控】细胞治疗产品生产过程中应当采取措施尽可能防止污染和交叉污染,如:
第三十条 【微生物污染的处理】应当制定监测各生产工序微生物污染的操作规程,并规定所采取的措施,包括评估微生物污染对产品质量的影响,确定消除污染并可恢复正常生产的条件。处理被污染的产品或物料时,应当对生产过程中检出的外源微生物进行鉴别,必要时评估其对产品质量的影响。应当保存生产中所有微生物污染和处理的记录。
第三十一条 【生产中混淆和差错的防控】细胞治疗产品生产过程中应当采取措施尽可能防止混淆和差错,如:
第三十二条 【及时目检】细胞治疗产品生产用包装容器及其连接容器(如有)应当在使用前和灌装后立即进行目检,以确定是否有损坏或污染迹象。
第三十三条 【一次性耗材】直接接触细胞治疗产品的无菌耗材应当尽可能使用一次性材料。
第三十四条 【中间品转运】生产过程中的中间产品和物料的转运有特殊要求的,如温度,应当对转运条件有明确的规定,并有相应的转运记录。
第七章 质量管理
第三十五条 【留样】无法使用成品留样的,可选择与成品相同成分的中间产品留样,留样包装、留样保存条件及留样期限应当满足留样的目的和要求。因满足临床必需而无法留样的,应当在批记录中附有成品的照片,能够清晰体现成品标签的完整信息。
第三十六条 【产品放行前质量评价】细胞治疗产品放行前的质量评价应当确认每批产品的信息完整、正确且可追溯,否则不得放行。
第三十七条 【有条件放行产品】发生危及患者生命的紧急情况而必须提供检验结果未达到放行质量标准的产品时,企业应当联系医疗机构,获得医疗机构书面同意和患者的知情同意书,并经企业专人医学评价,认为患者用药的受益大于风险,且产品的安全性指标符合放行质量标准的,可有条件放行该批产品。有条件放行批次产品的医疗机构书面同意、患者的知情同意书和企业医学评价,以及放行后可能增加的额外检验记录和报告,均应当纳入该批记录中。企业应当将有条件放行批次产品的质量情况、医疗机构的评估情况和患者用药后的情况,按年度书面报告给省级药品监督管理部门。
第三十八条 【记录保存】细胞治疗产品的批记录应当至少保存至产品有效期后五年。采用异体供体材料生产的细胞治疗产品,其批记录应当长期保存。
第三十九条 【不合格品和过期留样产品的处理】应当建立安全、有效处理不合格供体材料、中间产品、成品、过期留样样品的操作规程,处理应当有记录。
第四十条 【质量缺陷的处理】企业获知细胞治疗产品在运输和使用过程中发现有质量缺陷,如包装袋破损、标签信息错误和脱落,或者产品温度在运输过程中超标,应当立即启动应急处理并展开调查,相关应急处理和调查应当有记录和报告。必要时还应当启动产品召回。有质量缺陷但不涉及安全性指标的产品,如仍需临床使用,应参照第三十七条执行。
第八章 产品追溯系统
第四十一条 【产品追溯系统】企业应当建立产品标识和追溯系统,确保产品在供体材料接收、运输、生产和使用全过程中,来源于不同供体的产品不会发生混淆、差错,且可以追溯。该系统宜采用经验证的计算机化系统,应当可以实现对产品的双向追溯,包括从供体材料接收、运输、生产、检验和放行,直至成品运输和使用的全过程。
第四十二条 【唯一供体编号】企业应当对每一个供体编制具有唯一性的编号(或代码),用于标识供体材料和产品。
第四十三条 【书面操作规程】企业应当建立书面操作规程,规定供体材料和产品在接收、运输、生产、检验、放行、发放过程中正确标识与核对标识信息的操作和记录,确保可识别供体且具有唯一性的编号(或代码)不会发生标识错误或遗漏,且具有可追溯性。
第四十四条 【信息交流】企业应当与医疗机构建立信息交流机制,及时交流供体材料采集、产品使用及与产品质量相关的关键信息等,必要时采取相应的措施。
第九章 供体材料的采集和产品的使用
第四十五条 【医疗机构资格】企业应当选择具有合法资质的医疗机构作为供体材料采集和产品使用的机构。质量管理部门应当对医疗机构进行质量评估,会同有关部门对医疗机构进行现场质量审计,以确保医疗机构供体材料的采集、产品的使用符合要求。质量管理部门对质量评估不符合要求的医疗机构应当行使否决权。
第四十六条 【对医疗机构的认可程序】企业应当建立对医疗机构进行质量评估和批准的操作规程,明确医疗机构的资质、选择的原则、质量评估方式、评估标准及合格医疗机构批准的程序,并明确现场质量审计的内容、周期、审计人员组成及资质。
第四十七条 【合格机构名单和质量档案】企业质量管理部门应当指定专人负责医疗机构的现场质量审计,分发经批准的合格医疗机构名单,并建立每家医疗机构的质量档案。
第四十八条 【质量协议】企业应当与经批准的合格医疗机构签订质量协议。质量协议的内容应当包括供体材料的采集方法、保存条件和质量标准。
第四十九条 【医疗机构资格取消】企业应当定期对医疗机构采集供体材料和使用产品的情况进行回顾和评估,一旦发现医疗机构出现不符合操作规程,且可能会对患者造成不利影响的情况,应当及时要求医疗机构采取纠正措施和预防措施,必要时不再纳入合格医疗机构名单。
第五十条 【采集操作规程】企业应当制定供体筛查标准,制订供体材料采集、运输、接收标准操作规程,详细说明供体材料的采集方法、保存和运输条件以及接收的标准。
第五十一条 【产品使用指导】企业应当制定详细的产品使用操作规程。产品在医疗机构使用前需要现场配制的,应当详细描述复苏方法、稀释清洗方法、配制的环境、无菌要求、暂存时间和温度、转运方式等,必要时可以图片或视频形式说明。
第五十二条 【培训】企业应当对医疗机构人员进行供体材料采集和产品使用的培训,培训应当有记录。
文章来源:GMP资料共享群
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。