扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
 文件目录
文件目录
一.目的
二.职责
三.定义
四.适用范围
五.程序
六.相关程序及记录
七.参考资料
八.附录
分发清单:
质量控制部、质量保证部
机密等级:
机密(仅限计算机化系统验证总群437487116内部使用)
一.目的
用于规范QC实验室产生的电子数据管理,确保数据信息的真实性、安全性和完整性。通过信息系统中采用的某种安全机制,规范不同权限的授权人进入后确保保密性,同时防止未授权的人员进入系统后对其中的记录进行更改或删除,消除人为错误和偶然的数据丢失。
二.职责
IT系统管理员
管理实验室所有计算机系统的管理员权限、软件系统的管理员权限和数据的备份。
仪器管理员
负责仪器的管理及维护保养,电子数据的审核,保证数据的唯一性和准确性。
化学家
负责检测方法的编辑和电子数据的审核。
分析员
软件系统的日常使用。
审核人员
审核人员在审核过程中不应对数据做出变动和修改,不能审核自己生成的数据。
部门经理
负责监督本规程的实施。
三.定义
权限:是指对设备和软件使用的操作权利,不同级别的权限可以操作的项目不同。
IT系统管理员:不进行实验操作。
电子数据:也称数据电文,是指以电子、光学、磁或者类似手段生成、发送、接收或者储存的信息。
数据完整性:是指数据的完全性、一致性和准确性。完全、一致和准确的数据应当具有可归属性、清晰可辨性、即时被记录、原始性或真实有效副本。
审计追踪:审计追踪是指安全的、计算机生成的、时间标记的电子记录。审计追踪是一份“谁、什么、何时和为什么”记录的时序表。例如,高效液相色谱(HPLC)运行的审计追踪包括用户名、运行日期/时间、使用的积分参数,以及再处理细节(如果存在的话),包括再处理的变更理由。
备份:指在整个记录保存期间安全地保存的原始数据的真实有效副本。
四.适用范围
本程序适用于XXXX公司质量控制部实验室所使用计算机系统及软件工作站的管理。
五.程序
5.1计算机系统
5.1.1实验室要控制无关人员的进入,实验室的所有电脑只允许本部门人员、IT系统管理员使用,其他任何人不得自行访问和使用,如确实有使用电脑的需要,必须经过QC负责人同意;
5.1.2建立数据系统逻辑安全体系,避免系统数据的误用、出错和伪造。实验室每台电脑均需设定系统登录密码和屏幕保护程序;
5.1.3实验室电脑应设置程序或采取措施,保证电脑的系统时间不能被更改。除IT系统管理员为“administrator”权限外,其余人员均为“user”权限;
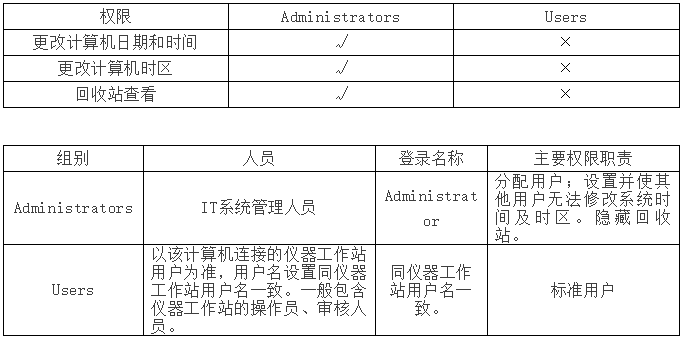
5.1.4计算机锁屏:操作人员离开电脑时需对电脑进行锁定(快捷键: Windows +L),无操作3分钟自动锁屏,恢复时使用密码保护。
5.1.5用户名及密码设置:
Ø 每个使用人建立一个账户,由本人姓名全拼作为账户名。
Ø 每个人的账户唯一并设置密码,密码不得少于6位数,由数字和大、小写字母组成,密码有效期不得超过90天。
Ø 密码三次错误输入之后,帐号锁定30分钟。
Ø 每个用户只能使用自己的用户名和密码登录,并且要管理好自己的账户和密码,严禁将自己的密码告知其他人员,严禁使用他人的用户名和密码登录。
Ø 新用户第一次使用,会被强制性要求更改密码,更改原则同5.1.5中第2条。
5.2软件系统
5.2.1工作站用户的建立
对于不同的仪器应进行用户权限分级管理。用户权限分为A、B、C、D、E级四级:系统管理员(A级)、仪器管理员(B级)、化学家(C级)、分析员(D级)、访问者(E级)。
A级:IT系统管理员,可以访问相应系统所有功能。负责工作站的全面监控。
B级:仪器管理员,负责仪器的管理和数据的审查。
C级:化学家,负责项目的建立,方法的编辑,数据的审查。
D 级:分析员,只能访问系统的部分功能。允许操作、访问与基本操作有关的系统功能。
E级:访问者,仅拥有访问数据、审查数据的权限。
各级用户具体权限详见QFXX《实验室工作站用户权限表》。
IT系统管理员依据QXX《工作站用户申请表》建立、修改或移除用户账户。
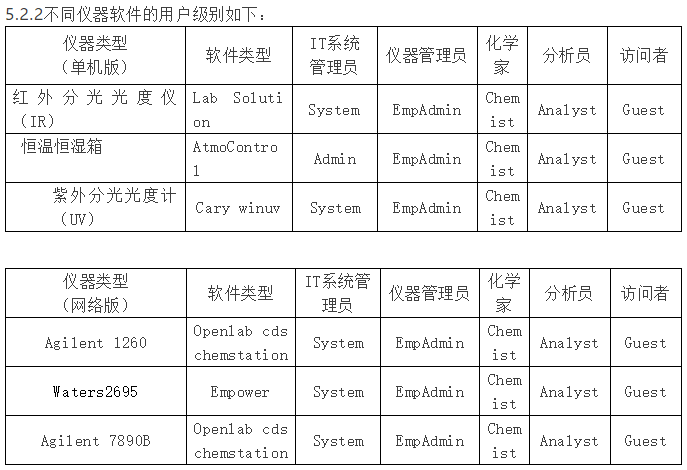
5.2.3对于厂家的维修工程师需要进行配置或为特定的仪器安装驱动程序,或者对仪器进行维护或认证等的时候,需要建立工程师专用账户,此用户经QC经理批准后由IT系统管理员创建,需要用到IT的权限时,工程师的工作必须在IT的监督下进行。 同时需要登记相关仪器维护台账,在工程师离开后,需要禁用此用户,工程师下次需要再进行相应操作时再“激活”此用户。
5.3电子数据的保存
3.1序列
序列表命名原则为产品名称-检测项目-检测日期-2位流水号(例如:双嘧达莫有关物质140420- 01表示2014年04月20日检测的双嘧达莫有关物质的第一个序列。
所有的序列文件均存储在相关工作站的“Sequence”文件夹
3.2方法
方法命名原则为产品名称-检测项目。所有方法文件均存储于相应工作站的“Method”文件夹
3.3数据文件
数据文件夹命名原则以产品中文名命名。涉及到其他检测,则命名原则如下:
3Q:生产厂家进行的IQ/OQ,用“IQ/OQ”表示,PQ用“PQ”表示。若软件要求厂家3Q 文件必须存在根目录下,可以将此项目放在根目录下。
内校:企业按照校验计划进行的定期校验,用“内校”或“Internal CAL”表示。
外校:企业按照计量计划进行的定期校验,用“外校”或“External CAL”表示。
培训:实验员培训内容,用“培训”或“Training”表示。
维修:仪器在内部或外部维修所做的测试,用“维修”或“Repairing”表示。
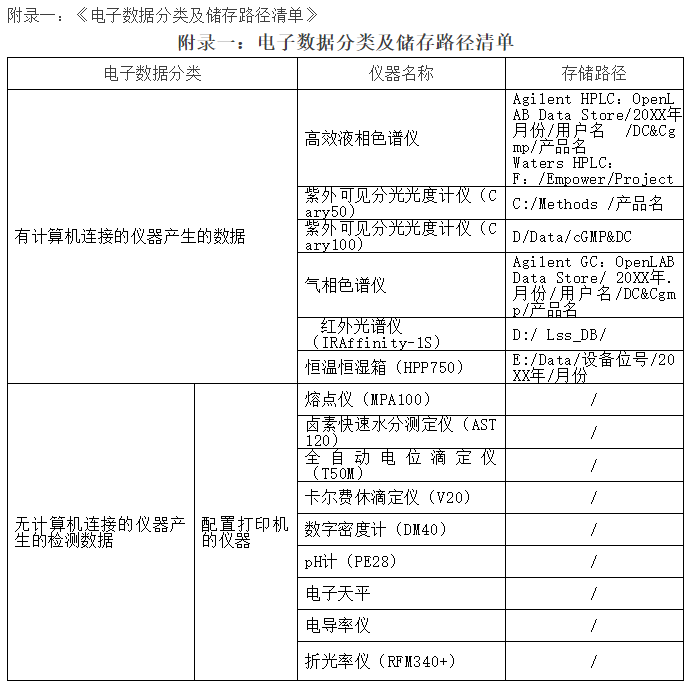
所有数据文件根据工作站不同存储路径有所不同,具体存储路径见附录一《电子数据分类及储存路径清单》。
5.3.4数据报告的打印
当图谱处理完成,即可生成数据报告,以安捷伦1260液相为例,报告的打印应包括以下内容:
样品信息
分析方法参数
样品序列报告
结果报告
其他仪器应参考此标准打印
5.4数据备份与归档:
5.4.1备份周期:服务器数据每天备份至专用的备用服务器中,每月异地备份,备份数据应标明日期、仪器编号、分析人员等。
5.4.2备份要求:备份对原始数据的备份。
单机版仪器产生的数据,将备份的数据拷贝至移动硬盘中,移动硬盘有A和B共 2个硬盘,每个盘中格式均为:仪器名称→设备位号→备份时间。备份完成后填写QF0567《数据备份与恢复记录》。A盘交给IT负责人进行归档,注明归档人和归档时间;B盘由质量保证部接收,储存在QA,并在记录上签字,保管。
5.5 电子数据的审核
5.5.1有计算机连接的仪器产生的数据审核。
5.5.1.1实验由HPLC、GC、IR、UV等产生的电子数据均需由经过培训的第二人进行审核。每批检验数据 (包括验证)需在放行前经数据审核人员全面核查。并填写QF0581《电子数据审核表(色谱类)》或QF0588《电子数据审核表(光谱类)》。具体审核人员、审核频次、数据审核的主要内容见下表:
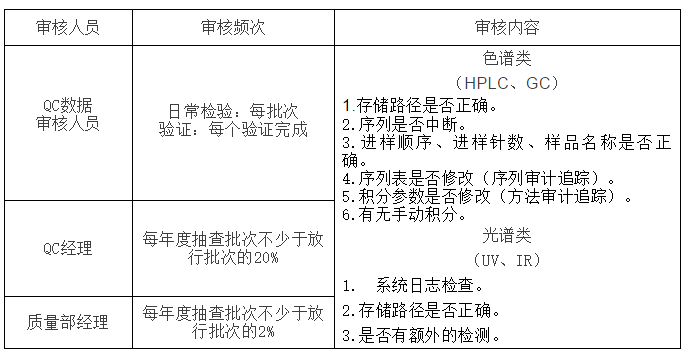
5.6电子数据整改:
5.6.1当发现数据存储路径错误时,须上报QC主管或经理,经其评估该情况对数据无影响后,由仪器管理员将数据移动至正确的存储位置,相关人员在使用记录上备注清楚路径的变化情况并签名。此类路径错误的数据应在保存至正确的路径后再进行处理。
5.6.2当发现命名错误后,须上报QC主管或经理,经检查确认后,将正确的命名在使用记录上备注签名,如具有相应的报告、图谱则需操作者划改订正并备注签名。
5.6.3当发现有重复进样、随意手动积分等不合理现象时候,立即上报QC经理,进行相应的调查,并制定相应的纠正和预防措施。
QF0565《色谱/光谱再处理表》
QF0568《工作站用户申请表》
QF0567《数据备份与恢复记录》
QF0569《实验室工作站用户权限表》
QF0581《电子数据审核表(色谱类)》
QF0588《电子数据审核表(光谱类)》
MHRA数据完整性指南
EU GMP ANNEX 11计算机化系统
CFDA GMP附录 计算机化系统
FDA工业指南part11的范围与应用
文章来源:药研技术汇
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。