扫一扫 添加小助手
服务热线
13818320332
扫一扫 关注我们
 1.目的:
1.目的:
本规程定义了 GMP 计算机及自动化系统关于数据备份恢复的基本通用规程。规程涉及了数据的产生,存储和归档,采用独立的物理介质备份机制以避免系统因意外事故,网络中断,病毒恶意攻击,系统或软件参数修改等造成重要数据的丢失。
2.范围:
本操作规程适用于公司所有GMP计算机和自动化系统的电子数据管理,此类系统用于或为GMP法规环境提供支持。
3.职责
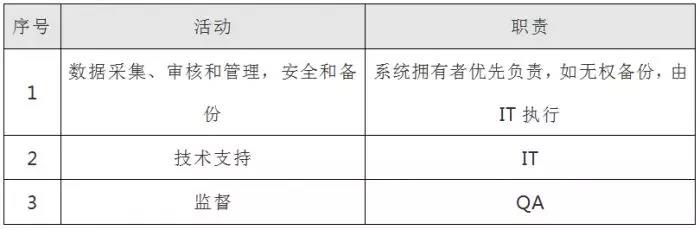
4.术语和定义
4.1备份/恢复:备份是指复制记录、数据和软件的过程,用以预防原始记录、数据和软件的完整性和可用性的损失。恢复是指随后在需要时还原己备份的记录、数据或软件
4.2存档:存档是指通过将记录和数据转移到另外的位置或系统,以使其不可在当前工作中使用的过程,这通常能使这些记录和数据不再变动。有时还需要同时保存支持这些记录和数据的应用程序。存档记录应该可以很容易地获取,以用于商业目的或监管目的。
5.程序
5.1应将计算机系统的数据和软件进行周期性的备份,并做好记录(见附件1)。所有备份介质存放在档案室,按照《档案管理规范(Q/CDGK3.18)》的相关要求进行管理,一律不准外借,不准流出公司,任何人员不得擅自取用,更不得私自再备份。归档的备份介质取用,需经质量负责人批准,并填写《档案借阅审批表》。借用人员使用完介质后,应立即归还,由档案管理员检查,确认介质完好。
5.2独立的数据文件,数据每次以独立的数据文件产生,可以由应用程序直接从磁盘分别调用,如HPLC Chemstation 产生的数据文件,这样文件的备份可以只备份新增的文件。
5.3文件型数据库的应用程序通常不提供备份功能,备份时需要从磁盘上直接复制数据库,比如Access 数据库。由于所有数据存贮与一个数据库内,需要对数据库全部复制。
5.4关系型数据库是同时存放数据及其关系的数据库,这些数据库通常由应用程序提供备份功能或自动备份功能,对于这类数据库应采用完全备份的方式进行备份,备份后的文件复制在备份磁盘上。
5. 5备份周期通常可以设定为一个月,如果程序自动备份,异地备份的周期可为一年。
5.6可通过备份前后文件或文件夹的大小、文件数量来核查被备份的文件或文件夹的完整性,并进行登记,表格见附件1。
5.7每半年应对之前的备份介质进行一次检查,应随机抽取至少一份备份介质,在该备份介质上调用至少1个备份数据,并打印相关报告,作为附件并登记,检查表格见附件2.
5.8存放备份数据的介质必须具有明确的标识;标识必须使用统一的命名规范,注明介质编号、介质的启用日期、保留期限和系统管理员等重要信息。
5.9本公司数据备份的介质通常选择光盘或移动硬盘,其使用和储存条件为:
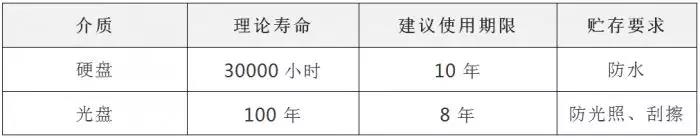
5.10如因系统或设备升级等原因,原记录和数据不再发生变化,可以将记录和数据转移到另外的位置或系统,同时保存支持这些记录和数据的应用程序,进行存档备份处理。存档备份的数据应该可以很容易地获取,以用于商业目的或监管目的。
备份文件的保存时间至少为产品效期后一年,出口的原料药保存时间为该批产品销售后三年。过期或不能使用的备份媒介应通过受控的方式进行销毁或处置,由数据使用部门和质量管理人员现场见证销毁或处置过程,并提供有签名的证明文件。
5.11系统出现故障或损坏时,可以由系统管理员调取备份的电子数据进行恢复。未及时进行备份的数据,经质量监督管理部门调查分析后,决定是否重新检验。包括系统故障和数据错误在内的所有事故都应当被记录和评估,重大的事故应当进行彻底调查,识别其根本原因,并采取相应的纠正措施和预防措施。
5.12在备份、归档和恢复过程中,出现的错误应详细记录在备份日志中,必要时报告偏差,并进行调查处理。
文章来源: CROU制药在线
本网站刊载的所有内容,包括文字、图片、音频、视频、软件等,如非标注为“原创”,则相关版权归原作者所有,如原作者不愿意在本网站刊登相关内容,请及时通知本站,我们将第一时间予以删除。